2025年1月13日,国家药监局核查中心重磅发布《细胞治疗产品生产检查指南》(以下简称《指南》),这一指南为细胞治疗产品领域带来了重要的规范与指引。一方面,它为细胞治疗产品生产企业提供了明确的操作规范和标准,有助于企业提高生产管理水平和产品质量;另一方面,也为监管部门提供了科学、规范的检查依据,使市场监管更具针对性和有效性。
《指南》从质量管理、厂房与设施设备、物料及产品、生产管理、质量控制、包装和标签、产品追溯系统、供者材料与医疗机构管理几个方面都进行了细致且严格的规范。下文将围绕细胞治疗产品的生产工艺及控制、质量控制的相关条例展开解读,并为生产企业提供泰林系统解决方案,助力企业更好地理解和应用《指南》。
生产工艺及控制
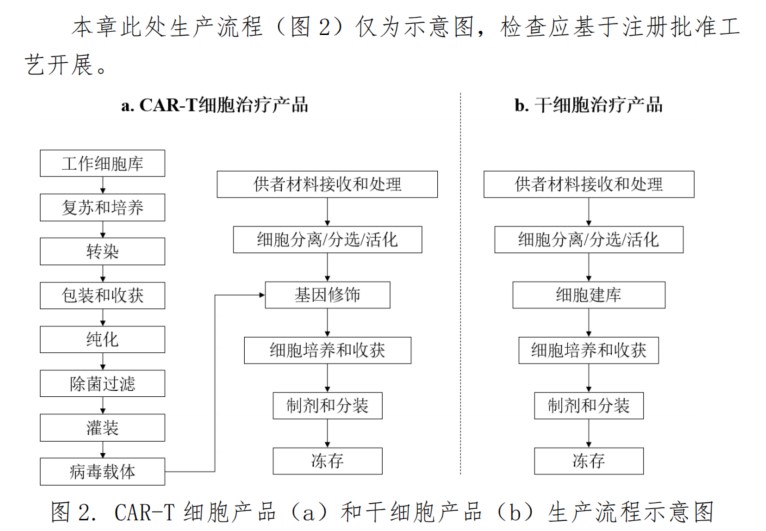
《指南》中列举了2种细胞产品生产流程示意图,但不同细胞治疗产品工艺存在差异,检查员应按照注册批准证明文件批准的工艺开展检查。需强调的是,细胞治疗产品为无菌生产工艺,生产的无菌保证及控制尤其重要。同时,生产过程用到大量一次性无菌耗材,关键耗材使用前应确认其完整性,并关注对耗材可见异物的控制措施。


隔离器是细胞治疗产品生产的常见设备,是无菌生产的必要条件,《指南》中对隔离器的要求主要包括以下几个方面:
1、设备构成与内部环境:一般含操作舱和传递舱;隔离器内部环境应达到A级洁净度级别,关键区域有初始气流保护;
2、性能确认:需对隔离器性能进行确认,确认状态应与实际生产工艺需求相符合;
3、环境监测:制定环境监测措施,操作舱体内实现在线监测,监测有记录并可追溯;
4、清洁消毒与检查:每批次生产前,对隔离器内舱体进行消毒和清洁;定期检查隔离器的密封完整性;按要求进行手套完整性测试;关注批次间切换的防污染措施及有效性评估;
5、无菌状态维持时长:应确认隔离器的无菌状态维持时长。

细胞制备隔离器
泰林细胞制备隔离器是专门用于细胞产品制备,并满足GMP无菌化生产要求的密闭式集成化操作系统,可代替传统GMP实验室,集成细胞分离、激活、修饰、扩增、观察、收集分装等功能设备,并为细胞产品提供持续的无菌操作环境。包括全过程A级洁净环境、一键式正负压操作模式切换、全方位H2O2消毒、数据实时监控可追溯、21天长时间无菌环境维持等功能,可完美适配《指南》要求。


蜂巢培养箱是由蜂巢式多工位模块和配套的培养箱组成,为细胞培养的常用设备,在《指南》中也有较详细的阐述,主要包括设备构成与内部环境要求、设备电源要求、气源要求、参数和性能的确认等。

蜂巢式细胞培养系统
泰林蜂巢式细胞培养系统满足GMP无菌化生产要求,为细胞产品提供高智能化持续的无菌培养环境。蜂巢式细胞培养系统为转运升降小车和蜂巢式细胞培养站组合,可满足大规模、多样本量的细胞培养要求。泰林蜂巢式培养箱箱门为充气密封形式,对接灭菌采用VHP自动灭菌,培养过程可直接观察,方形培养箱可实现高空间利用率;配备转运小车一键升降灵活对接,保障全流程无菌。此外,该系统满足系统控制和环境监控数据实时记录并储存、生产培养全过程的数据可追溯、识别每个独立培养单元并可进行批次管理等功能。
泰林细胞制备隔离器与蜂巢式细胞培养系统组合为泰林细胞制备工作站,专用于细胞产品的培养和制备,符合中国GMP细胞治疗产品的附录、中国GMP无菌产品生产、中国细胞治疗产品研究与技术评价指导原则、FDA/EMA/NMPA和ISO/PDA/USA/中国药典等法规的要求。

质量控制
细胞治疗产品是一类“活细胞药物”,具有起始细胞来源及类型多样、批次规模小、全程无菌生产、最终制剂成品批量小、临床使用需求急迫等特点,故细胞治疗产品的质量特征有别于其他化学药品和生物制品。
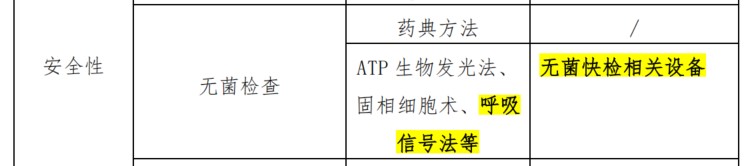
无菌检查是细胞治疗产品的必要质量检验项目,其主要检测方法包括药典法、ATP生物发光法、固相细胞术和呼吸信号法等。《9406细胞类制品微生物检查指导原则》中指出,由于细胞治疗产品的特殊性,在风险评估的基础上有条件地采用快速微生物检查法替代经典无菌检查法(药典法)已成为安全性质控的必要手段,该指导原则也将呼吸信号法作为快速微生物检查的推荐方法。

无菌检查隔离器
无菌检查隔离器可为无菌操作提供GMP A级环境,最大程度减少微生物污染风险。泰林新一代隔离器产品—TECHLEAD®CST系列无菌隔离器,采用全新一代VHPS灭菌技术,实现过氧化氢浓度和饱和度可控,缩短了传递舱和操作舱灭菌时间,创造持续的GMP A级洁净环境;优化气流处理系统设计,排残时间缩短;依据GAMP5指南设计的智能化控制系统,新增多项监测参数,具有多级定制化权限控制;可集成如快速灭菌传递舱、集菌仪等功能模块和配置。符合中国GMP和中国药典以及EUGMP/FDA cGMP/USP-NF要求。

全自动无菌检查培养系统
泰林全自动无菌检查培养系统,基于呼吸信号法,是细胞制品快速无菌检查的不二之选。该系统可实时监测培养器底部感应器颜色的变化(由微生物代谢产生的CO2引起),计算机系统进行分析并转换为生长信号,采用专用算法来判断无菌检查结果。该系统最快可在8小时内获得阳性判读结果;支持直接接种法和薄膜过滤法;2~3个培养室,具有单独控温模块;针对含抗生素类检品提供专用培养瓶以有效避免假阴性风险。符合中国药典<9406>细胞类制品微生物检查指导原则和USP/EP/FDA相关法规要求。
总结
《细胞治疗产品生产检查指南》的正式发布,无疑是细胞治疗领域的一个重要里程碑,它为整个行业筑牢了规范基石,从生产到质量把控,全方位引领着细胞治疗产品行业走向标准化、科学化。而泰林的一系列系统解决方案都精准契合《指南》要求,为细胞治疗产品生产企业提供了有力支持,助力企业在满足法规标准的同时,不断提升产品质量与生产效率,共同推动细胞治疗产品行业稳健前行。
